


研究发现肝细胞癌治疗新靶点
近日,中国科学院合肥物质科学研究院研究员杨武林团队,揭示了肝细胞癌(肝癌)与良性肝再生过程的代谢机制的差异,发现通过联合靶向特定代谢酶与维生素A衍生物,可实现比现有靶向药物更高效的肝癌抑制效果,为肝癌治疗开辟了新路径。
肝细胞癌的恶性增殖机制与正常肝组织再生修复过程存在差异。传统治疗手段易产生耐药性且副作用明显,因此亟需研发更精准的治疗策略。科研团队对比肝癌细胞与良性再生肝细胞的基因表达差异,锁定六个关键代谢酶来开展研究。研究显示,这些酶在肝癌中异常活跃,推动癌细胞快速合成生物大分子,并实现恶性增殖。其中,ATP柠檬酸裂解酶、葡萄糖-6-磷酸脱氢酶、胸苷酸合成酶位于代谢通路上游,成为抑制肝癌增殖的“黄金靶点”。同时,研究发现,肝癌细胞中视黄醇代谢通路受阻,导致其代谢产物视黄酸水平下降,而视黄酸恰好是抑制肿瘤干细胞自我更新的关键因子。
基于上述发现,团队设计出“代谢酶抑制剂+视黄酸”联合疗法。通过特异性抑制前述三种代谢酶阻断癌细胞“能量工厂”,同时补充视黄酸抑制肿瘤干细胞再生。实验显示,这一组合疗法在体外实验中可抑制肝癌细胞增殖,并在动物模型中更展现出比索拉非尼更强的肿瘤抑制效果。
这一研究克服了传统单靶点治疗的局限,通过精准打击肝癌代谢网络中的多个关键节点,实现了抑制增殖到阻断再生的双重作用。该成果为肝癌治疗提供了新的联合用药策略,并为其他代谢异常相关癌症的研究提供了范式。
相关研究成果发表在《国际生物大分子杂志》上。
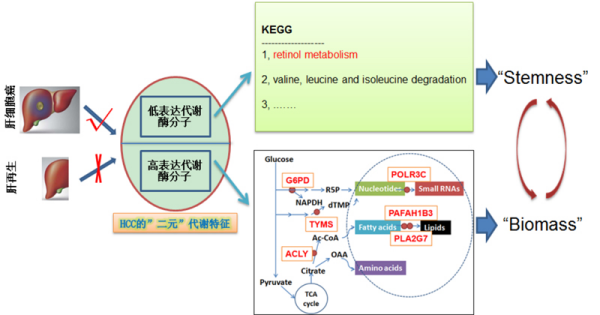
干预靶点调控机制示意图

延伸阅读
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性。
如果作者不希望被转载,请与我们联系。
如果作者不希望被转载,请与我们联系。





